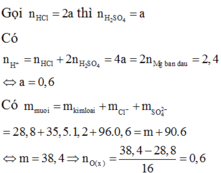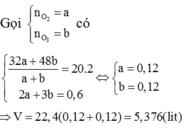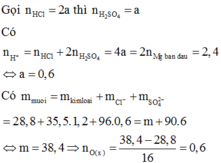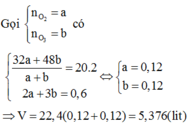Cho 3,36l hỗn hợp X: O2, O3 có dX/H2 = 56/3 vào bình đựng m (g) Mg vừa đủ, nhiệt độ -> m1(g) oxit. Tính m, m1

Những câu hỏi liên quan
Cho 3,36l hỗn hợp X: O2, O3 có dX/H2 = 56/3 vào bình đựng m (g) Mg vừa đủ, nhiệt độ -> m1(g) oxit. Tính m, m1
\(Gọi\ n_{O_2} = a(mol) ; n_{O_3} = b(mol)\\ n_X = a + b = \dfrac{3,36}{22,4} = 0,15(mol)\\ m_X = 32a + 48b = 0,15.\dfrac{56}{3}.2 =5,6(gam)\\ \Rightarrow a = 0,1 ; b = 0,05\\ O_2 + 4e\to 2O^{2-}\\ O_3 +6e \to 3O^{2-}\\ Mg \to Mg^{2+} + 2e\\\)
Bảo toàn electron :
\(n_{Mg} = \dfrac{0,1.4 + 0,05.6}{2} = 0,35(mol)\\ \Rightarrow m = 0,35.24 = 8,4(gam)\\ n_{MgO} = n_{Mg} = 0,35(mol)\\ \Rightarrow m_1 = 0,35.40 = 14(gam)\)
Đúng 2
Bình luận (0)
Cho 6,72 lít (đktc) hỗn hợp X gồm O 2 , C l 2 có d X / H 2 = 22 , 5 tác dụng vừa đủ với m (g) hỗn hợp Y gồm Al và Zn thu được 31,9 gam hỗn hợp B gồm muối clorua và oxit của 2 kim loại. Tính m và %m mỗi chất trong Y?
Cho X là hỗn hợp gồm Na và Ca. m1(g) X tác dụng vừa đủ với V (1) dung dịch HCl 0,5M thu được 3,36 (lít) H2 (đktc). m2 (g) X tác dụng vừa đủ với 10,8 (g) nước. Tính: a) Tỉ lệ khối lượng m1/m2 b) Nếu cho m2 (g) X tác dụng vừa đủ với V dung dịch HCl thì nồng độ mol/lẩu dung dịch HCl đã dùng là bao nhiêu Không chép lại rồi trả lời
a) Coi X là kim loại R hóa trị n
\(2R + 2nHCl \to 2RCl_n + nH_2\\ n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow n_R = \dfrac{2}{n}n_{H_2} = \dfrac{0,3}{n}(mol)\\ 2R + 2nH_2O \to 2R(OH)_n + nH_2\\ n_{H_2O} = \dfrac{10,8}{18} = 0,6(mol)\\ \Rightarrow n_R = \dfrac{1}{n}n_{H_2O} = \dfrac{0,6}{n}(mol)\\ \)
Suy ra: \(\dfrac{m_1}{m_2} = \dfrac{0,3}{n} : \dfrac{0,6}{n} = \dfrac{1}{2}\)
b)
\(m_2 =2m_1 \\ \Rightarrow C_{M_{HCl\ TN_2}} = 2C_{M_{HCl\ TN_1}} = 0,5.2 = 1M\)
Đúng 3
Bình luận (0)
Oxi hóa 28,8 g Mg bằng V lít hỗn hợp khí A (đktc) gồm O2 và O3 có tỉ khối hơi đối với H2 là 20 thu được m gam hỗn hợp X gồm Mg và MgO. Hòa tan hoàn toàn hỗn hợp X bằng một lượng vừa đủ dung dịch hỗn hợp HCl chứa (m + 90,6) gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Giá trị của V là A. 6,272 lít B. 1,344 lít C. 5,376 lít D. 2,688 lít
Đọc tiếp
Oxi hóa 28,8 g Mg bằng V lít hỗn hợp khí A (đktc) gồm O2 và O3 có tỉ khối hơi đối với H2 là 20 thu được m gam hỗn hợp X gồm Mg và MgO. Hòa tan hoàn toàn hỗn hợp X bằng một lượng vừa đủ dung dịch hỗn hợp HCl chứa (m + 90,6) gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Giá trị của V là
A. 6,272 lít
B. 1,344 lít
C. 5,376 lít
D. 2,688 lít
Oxi hóa 28,8 g Mg bằng V lít hỗn hợp khí A (đktc) gồm O2 và O3 có tỉ khối hơi đối với H2 là 20 thu được m gam hỗn hợp X gồm Mg và MgO. Hòa tan hoàn toàn hỗn hợp X bằng một lượng vừa đủ dung dịch hỗn hợp HCl chứa (m + 90,6) gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Giá trị của V là A. 6,272 lít B. 1,344 lít C. 5,376 lít D. 2,688 lít
Đọc tiếp
Oxi hóa 28,8 g Mg bằng V lít hỗn hợp khí A (đktc) gồm O2 và O3 có tỉ khối hơi đối với H2 là 20 thu được m gam hỗn hợp X gồm Mg và MgO. Hòa tan hoàn toàn hỗn hợp X bằng một lượng vừa đủ dung dịch hỗn hợp HCl chứa (m + 90,6) gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Giá trị của V là
A. 6,272 lít
B. 1,344 lít
C. 5,376 lít
D. 2,688 lít
Cần vừa đủ m1 gam O2 để đốt cháy hoàn toàn m2 gam hỗn hợp X gồm Cu và Al, thu được 28,4 gam hỗn hợp 2 oxit của Cu và Al có tỉ lệ mol lần lượt là 1:2.
a. Viết PTHH.
b. Tính m1 và m2
ta có : 80x+102.2x=28,4
=>x=0,1 mol
2Cu+O2-to>2CuO
0,1----------------0,1
4Al+3O2-to>2Al2O3
0,1----------------0,2
=>m1=0,1.64=6,4g
=>m2=0,1.27=2,7g
Đúng 3
Bình luận (0)
Gọi số mol của CuO và Al2O3 lần lượt là x và y
Ta có:
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
x 0,5x x ( mol)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
y 0,75 0,5 y (mol)
theo tỉ lệ số mol của Cu và Al ta có:
\(\dfrac{nCu}{nAl}=\dfrac{1}{2}\)
= > \(2nCu=nAl\)
=> \(2x-y=0\)
Ta có hệ pt theo đề bài:
\(\left\{{}\begin{matrix}64x+27y=28,4\\2x-y=0\end{matrix}\right.\)
giải hệ pt x và y lẽ đề ..
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 0,92 gam hỗn hợp X gồm C2H4, H2, C3H6, CO, C4H8 bằng O2 vừa đủ rồi cho toàn bộ sản phẩm cháy vào bình đựng 2 lít dung dịch Ca(OH)2 0,02 M thấy xuất hiện m1gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y có khối lượng tăng 0,82 gam so với dung dịch Ca(OH)2 ban đầu. Thêm từ từ dung dịch Ba(OH)2 vào dung dịch Y đến khi kết tủa hết các ion kim loại, thấy có m2 gam kết tủa. Biết m1 + m2 6,955, tính thành phần phần trăm theo khối lượng của CO và H2 có trong hỗn hợp X.
Đọc tiếp
Đốt cháy hoàn toàn 0,92 gam hỗn hợp X gồm C2H4, H2, C3H6, CO, C4H8 bằng O2 vừa đủ rồi cho toàn bộ sản phẩm cháy vào bình đựng 2 lít dung dịch Ca(OH)2 0,02 M thấy xuất hiện m1gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y có khối lượng tăng 0,82 gam so với dung dịch Ca(OH)2 ban đầu. Thêm từ từ dung dịch Ba(OH)2 vào dung dịch Y đến khi kết tủa hết các ion kim loại, thấy có m2 gam kết tủa. Biết m1 + m2 = 6,955, tính thành phần phần trăm theo khối lượng của CO và H2 có trong hỗn hợp X.

C2H4, C3H6, C4H8 cùng là anken nên có công thức chung là CnH2n
2CO + O2 → 2CO2↑ (1)
x → x (mol)
2H2 + O2 → 2H2O (2)
y → y (mol)
CnH2n + O2 → nCO2 + 2nH2O (3)
Sản phẩm cháy thu được gồm có CO2 và H2O.
Khi hấp thụ vào dd Ca(OH)2: 0,04 mol thu được dung dịch Y, thêm từ từ Ba(OH)2 vào dung dịch Y thu được kết tủa của các ion kim loại => CO2 phản ứng với Ca(OH)2 theo phương trình:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (4)
CO2 + Ca(OH)2 → Ca(HCO3)2 + H2O (5)
Dd Y chứa Ca(HCO3)2
BaCl2 + Ca(HCO3)2 → CaCO3↓ + BaCO3↓ + H2O (6)
m1 = mCaCO3(4)
m2 = mCaCO3(5) + mBaCO3
=> m1 + m2 = ∑ mCaCO3↓ + mBaCO3 = 6,955 (g) (*)
BTNT Ca: => ∑nCaCO3↓ = ∑ nCa(OH)2 (4+5) = 0,04 (mol)
Từ (*)

=> nCaCO3(6) = nBaCO3 = 0,015 (mol)
=> nCaCO3(4) = ∑nCa(OH)2 – nBaCO3 = 0,04 – 0,015 = 0,025 (mol)
BTNT C => ∑ nCO2 = ∑ nCaCO3 + nBaCO3 = 0,04 + 0,015 = 0,055 (mol)
Khối lượng dd Y tăng 0,82 gam so với dd Ca(OH)2 ban đầu
=> mCO2 + mH2O – mCaCO3(4) = 0,82
=> mH2O = 0,82 + 0,025.100 – 0,055.44 = 0,9 (g)
=> nH2O = 0,9 : 18 = 0,05 (mol)
BTKL ta có: mhhX + mO2 = mCO2 + mH2O
=> mO2 = 0,055.44 + 0,9 – 0,92 = 2,4 (g) => nO2 = 0,075 (mol)
BTNT O: nO( trong CO) + 2nO2 = 2nCO2 + nH2O
=> nO( trong CO) = 2.0,055 + 0,05 – 0,075.2 = 0,01 (mol) => nCO = 0,01 (mol)
Từ PTHH (1), (2), (3) ta thấy khi đốt cháy CnH2n luôn cho nH2O = nCO2 => sự chênh lệch mol CO2 và mol H2O là do đốt cháy CO và H2
=> nCO2 – nH2O = x – y = 0,055 – 0,05 = 0,005 (mol)
Mặt khác: nCO – nH2 = x – y = 0,005 (mol)
=> nH2 = nCO – 0,005= 0,01 – 0,005 = 0,055 (mol)
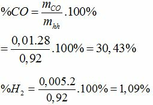
Đúng 0
Bình luận (0)
hỗn hợp X gồm CO và CO2 có tỉ khối hơi so với H2 là 16 .Cho m1 g X đi qua các ống đựng các oxit Al2O3,Fe2O3,CuO.kẾT thúc phản ứng thấy m g chất răn thu được giảm 2,4 g so với m g chất rắn ban đầu và V l CO2(đktc).Hấp thụ hết V l khí Co2' vaof 100 ml dung dịch nước vôi trong 1,5M KẾT THÚC PHẢN ỨNG THU ĐƯỢC m2 g kết tủa.Tính m1,m2,V
Cho m gam hỗn hợp gồm Mg, Al và Zn phản ứng vừa đủ với 7,84 lít (đktc) khí Cl2. Cũng m gam hỗn hợp trên phản ứng vừa đủ với m1 gam dung dịch HCl 14,6%. Giá trị của m1 là A. 87,5 B. 175,0 C. 180,0 D. 120,0
Đọc tiếp
Cho m gam hỗn hợp gồm Mg, Al và Zn phản ứng vừa đủ với 7,84 lít (đktc) khí Cl2. Cũng m gam hỗn hợp trên phản ứng vừa đủ với m1 gam dung dịch HCl 14,6%. Giá trị của m1 là
A. 87,5
B. 175,0
C. 180,0
D. 120,0
Đáp án B
Khi phản ứng với Cl2
n C l 2 = 7 , 84 22 , 4 = 0 , 35 ( m o l )
X – ne → X +n Cl2+ 2e→ 2Cl-
ne (KL nhường) = ne ( Cl2 nhận ) = 0,35.2 = 0,7 (mol)
Khi phản ứng với HCl
X – ne → X +n 2H+ + 2e → H2
ne( H+ nhận ) = ne (KL nhường) = 0,7 (mol)
=> nH+ = 0,7 (mol)
=> mHCl = 0,7.36,5 = 25,55 (g)
m d d H C l = m H C l . 100 % C % = 25 , 55 . 100 % 14 , 6 % = 175 ( g )
Đúng 0
Bình luận (0)